╨Ю╨а╨У╨Р╨Э╨Ш╨з╨Х╨б╨Ъ╨Р╨п ╨е╨Ш╨Ь╨Ш╨п2. ╨Р╨╗╨║╨░╨╜╤Л ╨╕ ╤Ж╨╕╨║╨╗╨╛╨░╨╗╨║╨░╨╜╤Л╨Т ╤Б╨╛╨╛╤В╨▓╨╡╤В╤Б╤В╨▓╨╕╨╕ ╤Б╨╛ ╤Б╤В╤А╨╛╨╡╨╜╨╕╨╡╨╝ ╤Г╨│╨╗╨╡╤А╨╛╨┤╨╜╨╛╨│╨╛ ╤Б╨║╨╡╨╗╨╡╤В╨░ ╤Г╨│╨╗╨╡╨▓╨╛╨┤╨╛╤А╨╛╨┤╤Л ╨┤╨╡╨╗╤П╤В ╨╜╨░ ╨░╨╗╨╕╤Д╨░╤В╨╕╤З╨╡╤Б╨║╨╕╨╡ (╤Б ╨╛╤В╨║╤А╤Л╤В╨╛╨╣ ╤Г╨│╨╗╨╡╤А╨╛╨┤╨╜╨╛╨╣ ╤Ж╨╡╨┐╤М╤О) ╨╕ ╤Ж╨╕╨║╨╗╨╕╤З╨╡╤Б╨║╨╕╨╡ (╤Б ╨╖╨░╨╝╨║╨╜╤Г╤В╨╛╨╣ ╤Г╨│╨╗╨╡╤А╨╛╨┤╨╜╨╛╨╣ ╤Ж╨╡╨┐╤М╤О). ╨Т ╨╖╨░╨▓╨╕╤Б╨╕╨╝╨╛╤Б╤В╨╕ ╨╛╤В ╤В╨╕╨┐╨░ ╤Б╨▓╤П╨╖╨╡╨╣ ╨╝╨╡╨╢╨┤╤Г ╨░╤В╨╛╨╝╨░╨╝╨╕ ╤Г╨│╨╗╨╡╤А╨╛╨┤╨░ ╨║╨░╨║ ╨░╨╗╨╕╤Д╨░╤В╨╕╤З╨╡╤Б╨║╨╕╨╡, ╤В╨░╨║ ╨╕ ╤Ж╨╕╨║╨╗╨╕╤З╨╡╤Б╨║╨╕╨╡ ╤Г╨│╨╗╨╡╨▓╨╛╨┤╨╛╤А╨╛╨┤╤Л ╨┤╨╡╨╗╤П╤В╤Б╤П ╨╜╨░ ╨╜╨░╤Б╤Л╤Й╨╡╨╜╨╜╤Л╨╡, ╤Б╨╛╨┤╨╡╤А╨╢╨░╤Й╨╕╨╡ ╤В╨╛╨╗╤М╨║╨╛ s -╤Б╨▓╤П╨╖╨╕, ╨╕ ╨╜╨╡╨╜╨░╤Б╤Л╤Й╨╡╨╜╨╜╤Л╨╡, ╤Б╨╛╨┤╨╡╤А╨╢╨░╤Й╨╕╨╡ ╨║╨░╨║ s ╤В╨░╨║ ╨╕ p -╤Б╨▓╤П╨╖╨╕.
╨Ъ ╨╜╨░╤Б╤Л╤Й╨╡╨╜╨╜╤Л╨╝ ╤Г╨│╨╗╨╡╨▓╨╛╨┤╨╛╤А╨╛╨┤╨░╨╝ ╨┐╤А╨╕╨╜╨░╨┤╨╗╨╡╨╢╨░╤В ╨░╨╗╨║╨░╨╜╤Л ╨╕ ╤Ж╨╕╨║╨╗╨╛╨░╨╗╨║╨░╨╜╤Л.
╨Р╨╗╨║╨░╨╜╤Л. ╨Р╨╗╨║╨░╨╜╤Л ╤П╨▓╨╗╤П╤О╤В╤Б╤П ╨╜╨░╤Б╤Л╤Й╨╡╨╜╨╜╤Л╨╝╨╕, ╨╕╨╗╨╕ ╨┐╤А╨╡╨┤╨╡╨╗╤М╨╜╤Л╨╝╨╕, ╤Г╨│╨╗╨╡╨▓╨╛╨┤╨╛╤А╨╛╨┤╨░╨╝╨╕, ╨┐╨╛╤Б╨║╨╛╨╗╤М╨║╤Г ╨▓╤Б╨╡ ╤Б╨▓╨╛╨▒╨╛╨┤╨╜╤Л╨╡ ╨▓╨░╨╗╨╡╨╜╤В╨╜╨╛╤Б╤В╨╕ ╨░╤В╨╛╨╝╨╛╨▓ ╤Г╨│╨╗╨╡╤А╨╛╨┤╨░ ╨╖╨░╨╜╤П╤В╤Л (╨┐╨╛╨╗╨╜╨╛╤Б╤В╤М╤О тАЬ╨╜╨░╤Б╤Л╤Й╨╡╨╜╤ЛтАЭ) ╨░╤В╨╛╨╝╨░╨╝╨╕ ╨▓╨╛╨┤╨╛╤А╨╛╨┤╨░. ╨Р╨╗╨║╨░╨╜╤Л ╨╜╨░╨╖╤Л╨▓╨░╤О╤В ╤В╨░╨║╨╢╨╡ ╨╜╨░╤Б╤Л╤Й╨╡╨╜╨╜╤Л╨╝╨╕ ╤Г╨│╨╗╨╡╨▓╨╛╨┤╨╛╤А╨╛╨┤╨░╨╝╨╕, ╨╕╨╗╨╕ ╨┐╨░╤А╨░╤Д╨╕╨╜╨░╨╝╨╕ (╤В╨╡╤А╨╝╨╕╨╜ тАЬ╨┐╨░╤А╨░╤Д╨╕╨╜╤ЛтАЭ ╨╛╨╖╨╜╨░╤З╨░╨╡╤В тАЬ╨╕╨╝╨╡╤О╤Й╨╕╨╡ ╨╝╨░╨╗╨╛╨╡ ╤Б╤А╨╛╨┤╤Б╤В╨▓╨╛тАЭ)
╨Я╤А╨╛╤Б╤В╨╡╨╣╤И╨╕╨╝ ╨┐╤А╨╡╨┤╤Б╤В╨░╨▓╨╕╤В╨╡╨╗╨╡╨╝ ╨░╨╗╨║╨░╨╜╨╛╨▓ ╤Б╨╗╤Г╨╢╨╕╤В ╨╝╨╡╤В╨░╨╜ ╨б╨Э4. ╨Э╨░╤З╨╕╨╜╨░╤П ╤Б ╨╜╨╡╨│╨╛, ╨╝╨╛╨╢╨╜╨╛ ╨┐╨╛╤Б╤В╤А╨╛╨╕╤В╤М ╤А╤П╨┤, ╨▓ ╨║╨╛╤В╨╛╤А╨╛╨╝ ╨║╨░╨╢╨┤╤Л╨╣ ╨┐╨╛╤Б╨╗╨╡╨┤╤Г╤О╤Й╨╕╨╣ ╤Г╨│╨╗╨╡╨▓╨╛╨┤╨╛╤А╨╛╨┤ ╨╛╤В╨╗╨╕╤З╨░╨╡╤В╤Б╤П ╨╛╤В ╨┐╤А╨╡╨┤╤Л╨┤╤Г╤Й╨╡╨│╨╛ ╨╜╨░ ╨╛╨┤╨╜╤Г ╨│╤А╤Г╨┐╨┐╤Г ╨бH2. ╨Ю╨▒╤Й╨░╤П ╤Д╨╛╤А╨╝╤Г╨╗╨░ ╨│╨╛╨╝╨╛╨╗╨╛╨│╨╕╤З╨╡╤Б╨║╨╛╨│╨╛ ╤А╤П╨┤╨░ ╨░╨╗╨║╨░╨╜╨╛╨▓ ╨бn╨Э2n+2.
╨Я╨╛ ╤Б╨╕╤Б╤В╨╡╨╝╨░╤В╨╕╤З╨╡╤Б╨║╨╛╨╣ ╨╜╨╛╨╝╨╡╨╜╨║╨╗╨░╤В╤Г╤А╨╡ ╨Ш╨о╨Я╨Р╨Ъ ╨┐╨╡╤А╨▓╤Л╨╝ ╤З╨╡╤В╤Л╤А╨╡╨╝ ╤З╨╗╨╡╨╜╨░╨╝ ╨│╨╛╨╝╨╛╨╗╨╛╨│╨╕╤З╨╡╤Б╨║╨╛╨│╨╛ ╤А╤П╨┤╨░ ╨░╨╗╨║╨░╨╜╨╛╨▓ ╨┐╤А╨╕╤Б╨▓╨╛╨╡╨╜╤Л ╨╕╤Е ╨╕╤Б╤В╨╛╤А╨╕╤З╨╡╤Б╨║╨╕ ╤Б╨╗╨╛╨╢╨╕╨▓╤И╨╕╨╡╤Б╤П ╨╜╨░╨╖╨▓╨░╨╜╨╕╤П тАФ ╨╝╨╡╤В╨░╨╜, ╤Н╤В╨░╨╜, ╨┐╤А╨╛╨┐╨░╨╜, ╨▒╤Г╤В╨░╨╜. ╨Э╨░╨╖╨▓╨░╨╜╨╕╤П ╨╛╤Б╤В╨░╨╗╤М╨╜╤Л╤Е ╨░╨╗╨║╨░╨╜╨╛╨▓ ╤Б ╨╜╨╛╤А╨╝╨░╨╗╤М╨╜╨╛╨╣. ╤В. ╨╡. ╨╜╨╡╤А╨░╨╖╨▓╨╡╤В╨▓╨╗╨╡╨╜╨╜╨╛╨╣ ╤Г╨│╨╗╨╡╤А╨╛╨┤╨╜╨╛╨╣ ╤Ж╨╡╨┐╤М╤О, ╤Б╨╛╤Б╤В╨░╨▓╨╗╤П╤О╤В╤Б╤П ╨╕╨╖ ╨│╤А╨╡╤З╨╡╤Б╨║╨╛╨│╨╛ ╨╕╨╗╨╕ ╨╗╨░╤В╨╕╨╜╤Б╨║╨╛╨│╨╛ ╨╜╨░╨╖╨▓╨░╨╜╨╕╨╣ ╤З╨╕╤Б╨╗╨╕╤В╨╡╨╗╤М╨╜╨╛╨│╨╛, ╤Б╨╛╨╛╤В╨▓╨╡╤В╤Б╤В╨▓╤Г╤О╤Й╨╡╨│╨╛ ╤З╨╕╤Б╨╗╤Г ╨░╤В╨╛╨╝╨╛╨▓ ╤Г╨│╨╗╨╡╤А╨╛╨┤╨░ ╨▓ ╤Ж╨╡╨┐╨╕, ╤Б ╨┤╨╛╨▒╨░╨▓╨╗╨╡╨╜╨╕╨╡╨╝ ╤Б╤Г╤Д╤Д╨╕╨║╤Б╨░ -╨░╨╜. ╨в╨░╨║, ╨│╤А╨╡╤З╨╡╤Б╨║╨╛╨╡ ╨╜╨░╨╖╨▓╨░╨╜╨╕╨╡ ╤З╨╕╤Б╨╗╨╕╤В╨╡╨╗╤М╨╜╨╛╨│╨╛ 5 тАФ тАЬ╨┐╨╡╨╜╤В╨░тАЭ, ╨╛╤В╤Б╤О╨┤╨░ ╤Г╨│╨╗╨╡╨▓╨╛╨┤╨╛╤А╨╛╨┤ ╨б5╨Э12 ╨╜╨░╨╖╤Л╨▓╨░╨╡╤В╤Б╤П ╨┐╨╡╨╜╤В╨░╨╜. ╨Ф╨╗╤П ╤Н╤В╨╛╨│╨╛ ╨╢╨╡ ╤Б╨╛╨╡╨┤╨╕╨╜╨╡╨╜╨╕╤П ╨╝╨╛╨╢╨╜╨╛ ╨▓╤Б╤В╤А╨╡╤В╨╕╤В╤М ╨╜╨░╨╖╨▓╨░╨╜╨╕╨╡ ╨╜-╨┐╨╡╨╜╤В╨░╨╜, ╤З╤В╨╛ ╨┐╨╛╨┤╤З╨╡╤А╨║╨╕╨▓╨░╨╡╤В ╨╜╨░╨╗╨╕╤З╨╕╨╡ ╨╜╨╛╤А╨╝╨░╨╗╤М╨╜╨╛╨╣ ╤Ж╨╡╨┐╨╕.
╨Э╨░╤З╨╕╨╜╨░╤П ╤Б ╨▒╤Г╤В╨░╨╜╨░ ╨╕ ╨┤╨░╨╗╨╡╨╡ ╨┤╨╗╤П ╨║╨░╨╢╨┤╨╛╨│╨╛ ╨╜╨╛╤А╨╝╨░╨╗╤М╨╜╨╛╨│╨╛ ╨░╨╗╨║╨░╨╜╨░ ╤Б╤Г╤Й╨╡╤Б╤В╨▓╤Г╤О╤В ╤Б╤В╤А╤Г╨║╤В╤Г╤А╨╜╤Л╨╡ ╨╕╨╖╨╛╨╝╨╡╤А╤Л ╤Б ╤А╨░╨╖╨▓╨╡╤В╨▓╨╗╨╡╨╜╨╜╨╛╨╣ ╤Ж╨╡╨┐╤М╤О.
╨Р╤В╨╛╨╝╤Л ╤Г╨│╨╗╨╡╤А╨╛╨┤╨░ ╤А╨░╨╖╨╗╨╕╤З╨░╤О╤В╤Б╤П ╨┐╨╛ ╨╝╨╡╤Б╤В╨╛╨┐╨╛╨╗╨╛╨╢╨╡╨╜╨╕╤О ╨▓ ╤Ж╨╡╨┐╨╕. ╨Р╤В╨╛╨╝ ╤Г╨│╨╗╨╡╤А╨╛╨┤╨░, ╤Б╤В╨╛╤П╤Й╨╕╨╣ ╨▓ ╨╜╨░╤З╨░╨╗╨╡ ╤Ж╨╡╨┐╨╕, ╤Б╨▓╤П╨╖╨░╨╜ ╤В╨╛╨╗╤М╨║╨╛ ╤Б ╨╛╨┤╨╜╨╕╨╝ ╤Б╨╛╤Б╨╡╨┤╨╜╨╕╨╝ ╨░╤В╨╛╨╝╨╛╨╝ ╤Г╨│╨╗╨╡╤А╨╛╨┤╨░ ╨╕ ╨╜╨░╨╖╤Л╨▓╨░╨╡╤В╤Б╤П ╨┐╨╡╤А╨▓╨╕╤З╨╜╤Л╨╝. ╨Р╤В╨╛╨╝ ╤Г╨│╨╗╨╡╤А╨╛╨┤╨░, ╤Б╨▓╤П╨╖╨░╨╜╨╜╤Л╨╣ ╤Б ╨┤╨▓╤Г╨╝╤П ╨┤╤А╤Г╨│╨╕╨╝╨╕ ╨░╤В╨╛╨╝╨░╨╝╨╕ ╤Г╨│╨╗╨╡╤А╨╛╨┤╨░, ╨╜╨░╨╖╤Л╨▓╨░╨╡╤В╤Б╤П ╨▓╤В╨╛╤А╨╕╤З╨╜╤Л╨╝, ╤Б ╤В╤А╨╡╨╝╤П тАФ ╤В╤А╨╡╤В╨╕╤З╨╜╤Л╨╝, ╤Б ╤З╨╡╤В╤Л╤А╤М╨╝╤П тАФ ╤З╨╡╤В╨▓╨╡╤А╤В╨╕╤З╨╜╤Л╨╝. ╨Т ╨╝╨╛╨╗╨╡╨║╤Г╨╗╨░╤Е ╨╜╨╛╤А╨╝╨░╨╗╤М╨╜╤Л╤Е ╨░╨╗╨║╨░╨╜╨╛╨▓ ╤Б╨╛╨┤╨╡╤А╨╢╨░╤В╤Б╤П ╨┐╨╡╤А╨▓╨╕╤З╨╜╤Л╨╡ (╨╜╨░ ╨║╨╛╨╜╤Ж╨░╤Е ╤Ж╨╡╨┐╨╕) ╨╕ ╨▓╤В╨╛╤А╨╕╤З╨╜╤Л╨╡ (╨▓ ╤Ж╨╡╨┐╨╕) ╨░╤В╨╛╨╝╤Л ╤Г╨│╨╗╨╡╤А╨╛╨┤╨░. ╨в╤А╨╡╤В╨╕╤З╨╜╤Л╨╡ ╨╕ ╤З╨╡╤В╨▓╨╡╤А╤В╨╕╤З╨╜╤Л╨╡ ╨░╤В╨╛╨╝╤Л ╤Б╨╛╨┤╨╡╤А╨╢╨░╤В╤Б╤П ╤В╨╛╨╗╤М╨║╨╛ ╨▓ ╨░╨╗╨║╨░╨╜╨░╤Е ╤Б ╤А╨░╨╖╨▓╨╡╤В╨▓╨╗╨╡╨╜╨╜╨╛╨╣ ╤Ж╨╡╨┐╤М╤О. ╨Т╤Б╨╡ ╤Н╤В╨╕ ╨░╤В╨╛╨╝╤Л ╤Г╨│╨╗╨╡╤А╨╛╨┤╨░ ╨╜╨╡╤Б╨║╨╛╨╗╤М╨║╨╛ ╤А╨░╨╖╨╗╨╕╤З╨░╤О╤В╤Б╤П ╨┐╨╛ ╤А╨╡╨░╨║╤Ж╨╕╨╛╨╜╨╜╨╛╨╣ ╤Б╨┐╨╛╤Б╨╛╨▒╨╜╨╛╤Б╤В╨╕.
╨б╤В╤А╤Г╨║╤В╤Г╤А╨╜╨░╤П ╨╕╨╖╨╛╨╝╨╡╤А╨╕╤П ╨╛╨▒╤Г╤Б╨╗╨╛╨▓╨╗╨╕╨▓╨░╨╡╤В ╨╕ ╨╝╨╜╨╛╨│╨╛╨╛╨▒╤А╨░╨╖╨╕╨╡ ╤Г╨│╨╗╨╡╨▓╨╛╨┤╨╛╤А╨╛╨┤╨╜╤Л╤Е ╤А╨░╨┤╨╕╨║╨░╨╗╨╛╨▓. ╨г╨│╨╗╨╡╨▓╨╛╨┤╨╛╤А╨╛╨┤╨╜╤Л╨╣ ╤А╨░╨┤╨╕╨║╨░╨╗ ╨┐╨╛╨╗╤Г╤З╨░╨╡╤В╤Б╤П, ╨╡╤Б╨╗╨╕ ╨╛╤В ╨╝╨╛╨╗╨╡╨║╤Г╨╗╤Л ╨░╨╗╨║╨░╨╜╨░ ╨╛╤В╨╜╤П╤В╤М ╨╛╨┤╨╕╨╜ ╨░╤В╨╛╨╝ ╨▓╨╛╨┤╨╛╤А╨╛╨┤╨░. ╨н╤В╨╛╤В ╤В╨╡╤А╨╝╨╕╨╜ ╨╜╨╡ ╤Б╨╗╨╡╨┤╤Г╨╡╤В ╨┐╤Г╤В╨░╤В╤М ╤Б ╨┐╨╛╨╜╤П╤В╨╕╨╡╨╝ тАЬ╤Б╨▓╨╛╨▒╨╛╨┤╨╜╤Л╨╣ ╤А╨░╨┤╨╕╨║╨░╨╗тАЭ, ╤Е╨░╤А╨░╨║╤В╨╡╤А╨╕╨╖╤Г╤О╤Й╨╕╨╝ ╨░╤В╨╛╨╝ ╤Б ╨╜╨╡╤Б╨┐╨░╤А╨╡╨╜╨╜╤Л╨╝ ╤Н╨╗╨╡╨║╤В╤А╨╛╨╜╨╛╨╝.
╨Э╨░╨╖╨▓╨░╨╜╨╕╨╡ ╤А╨░╨┤╨╕╨║╨░╨╗╨░ ╨┐╤А╨╛╨╕╨╖╨▓╨╛╨┤╤П╤В ╨╛╤В ╨╜╨░╨╖╨▓╨░╨╜╨╕╤П ╤Б╨╛╨╛╤В╨▓╨╡╤В╤Б╤В╨▓╤Г╤О╤Й╨╡╨│╨╛ ╨░╨╗╨║╨░╨╜╨░ ╤Б ╨╖╨░╨╝╨╡╨╜╨╛╨╣ ╤Б╤Г╤Д╤Д╨╕╨║╤Б╨░ -╨░╨╜ ╨╜╨░ ╤Б╤Г╤Д╤Д╨╕╨║╤Б -╨╕╨╗. ╨Т ╨╛╨▒╤Й╨╡╨╝ ╨▓╨╕╨┤╨╡ ╤А╨░╨┤╨╕╨║╨░╨╗╤Л, ╨┐╤А╨╛╨╕╨╖╨▓╨╡╨┤╨╡╨╜╨╜╤Л╨╡ ╨╛╤В ╨░╨╗╨╕╤Д╨░╤В╨╕╤З╨╡╤Б╨║╨╕╤Е ╤Г╨│╨╗╨╡╨▓╨╛╨┤╨╛╤А╨╛╨┤╨╛╨▓, ╨╜╨░╨╖╤Л╨▓╨░╤О╤В ╨░╨╗╨║╨╕╨╗╤М╨╜╤Л╨╝╨╕ ╨╕ ╨╛╨▒╨╛╨╖╨╜╨░╤З╨░╤О╤В R.
╨Ш╨╖╨╛╨╝╨╡╤А╨╕╤П ╤А╨░╨┤╨╕╨║╨░╨╗╨╛╨▓ ╨╜╨░╤З╨╕╨╜╨░╨╡╤В╤Б╤П ╤Б ╨┐╤А╨╛╨┐╨░╨╜╨░, ╨┤╨╗╤П ╨║╨╛╤В╨╛╤А╨╛╨│╨╛ ╨▓╨╛╨╖╨╝╨╛╨╢╨╜╤Л ╨┤╨▓╨░ ╨╕╨╖╨╛╨╝╨╡╤А╨╜╤Л╤Е ╤А╨░╨┤╨╕╨║╨░╨╗╨░. ╨Х╤Б╨╗╨╕ ╨░╤В╨╛╨╝ ╨▓╨╛╨┤╨╛╤А╨╛╨┤╨░ ╨╛╤В╨╜╤П╤В╤М ╨╛╤В ╨┐╨╡╤А╨▓╨╕╤З╨╜╨╛╨│╨╛ ╨░╤В╨╛╨╝╨░ ╤Г╨│╨╗╨╡╤А╨╛╨┤╨░, ╤В╨╛ ╨┐╨╛╨╗╤Г╤З╨╕╤В╤Б╤П ╤А╨░╨┤╨╕╨║╨░╨╗ ╨┐╤А╨╛╨┐╨╕╨╗ (╨╜-╨┐╤А╨╛╨┐╨╕╨╗), ╨╡╤Б╨╗╨╕ ╨╛╤В ╨▓╤В╨╛╤А╨╕╤З╨╜╨╛╨│╨╛ тАФ ╨┐╨╛╨╗╤Г╤З╨╕╤В╤Б╤П ╤А╨░╨┤╨╕╨║╨░╨╗ ╨╕╨╖╨╛╨┐╤А╨╛╨┐╨╕╨╗.
╨д╨╕╨╖╨╕╤З╨╡╤Б╨║╨╕╨╡ ╤Б╨▓╨╛╨╣╤Б╤В╨▓╨░. ╨Т ╨╛╨▒╤Л╤З╨╜╤Л╤Е ╤Г╤Б╨╗╨╛╨▓╨╕╤П╤Е ╨┐╨╡╤А╨▓╤Л╨╡ ╤З╨╡╤В╤Л╤А╨╡ ╤З╨╗╨╡╨╜╨░ ╨│╨╛╨╝╨╛╨╗╨╛╨│╨╕╤З╨╡╤Б╨║╨╛╨│╨╛ ╤А╤П╨┤╨░ ╨░╨╗╨║╨░╨╜╨╛╨▓ (╨б1тАФ╨б4)тАФ ╨│╨░╨╖╤Л. ╨Э╨╛╤А╨╝╨░╨╗╤М╨╜╤Л╨╡ ╨░╨╗╨║╨░╨╜╤Л ╨╛╤В ╨┐╨╡╨╜╤В╨░╨╜╨░ ╨┤╨╛ ╨│╨╡╨┐╤В╨░╨┤╨╡╨║╨░╨╜╨░ (╨б5тАФ╨б17) тАФ ╨╢╨╕╨┤╨║╨╛╤Б╤В╨╕, ╨╜╨░╤З╨╕╨╜╨░╤П ╤Б ╨б18 ╨╕ ╨▓╤Л╤И╨╡ тАФ ╤В╨▓╨╡╤А╨┤╤Л╨╡ ╨▓╨╡╤Й╨╡╤Б╤В╨▓╨░. ╨Я╨╛ ╨╝╨╡╤А╨╡ ╤Г╨▓╨╡╨╗╨╕╤З╨╡╨╜╨╕╤П ╤З╨╕╤Б╨╗╨░ ╨░╤В╨╛╨╝╨╛╨▓ ╤Г╨│╨╗╨╡╤А╨╛╨┤╨░ ╨▓ ╤Ж╨╡╨┐╨╕, ╤В. ╨╡. ╤Б ╤А╨╛╤Б╤В╨╛╨╝ ╨╛╤В╨╜╨╛╤Б╨╕╤В╨╡╨╗╤М╨╜╨╛╨╣ ╨╝╨╛╨╗╨╡╨║╤Г╨╗╤П╤А╨╜╨╛╨╣ ╨╝╨░╤Б╤Б╤Л, ╨▓╨╛╨╖╤А╨░╤Б╤В╨░╤О╤В ╤В╨╡╨╝╨┐╨╡╤А╨░╤В╤Г╤А╤Л ╨║╨╕╨┐╨╡╨╜╨╕╤П ╨╕ ╨┐╨╗╨░╨▓╨╗╨╡╨╜╨╕╤П ╨░╨╗╨║╨░╨╜╨╛╨▓. ╨Я╤А╨╕ ╨╛╨┤╨╕╨╜╨░╨║╨╛╨▓╨╛╨╝ ╤З╨╕╤Б╨╗╨╡ ╨░╤В╨╛╨╝╨╛╨▓ ╤Г╨│╨╗╨╡╤А╨╛╨┤╨░ ╨▓ ╨╝╨╛╨╗╨╡╨║╤Г╨╗╨╡ ╨░╨╗╨║╨░╨╜╤Л ╤Б ╤А╨░╨╖╨▓╨╡╤В╨▓╨╗╨╡╨╜╨╜╤Л╨╝ ╤Б╤В╤А╨╛╨╡╨╜╨╕╨╡╨╝ ╨╕╨╝╨╡╤О╤В ╨▒╨╛╨╗╨╡╨╡ ╨╜╨╕╨╖╨║╨╕╨╡ ╤В╨╡╨╝╨┐╨╡╤А╨░╤В╤Г╤А╤Л ╨║╨╕╨┐╨╡╨╜╨╕╤П, ╤З╨╡╨╝ ╨╜╨╛╤А╨╝╨░╨╗╤М╨╜╤Л╨╡ ╨░╨╗╨║╨░╨╜╤Л.
╨Р╨╗╨║╨░╨╜╤Л ╨┐╤А╨░╨║╤В╨╕╤З╨╡╤Б╨║╨╕ ╨╜╨╡╤А╨░╤Б╤В╨▓╨╛╤А╨╕╨╝╤Л ╨▓ ╨▓╨╛╨┤╨╡, ╤В╨░╨║ ╨║╨░╨║ ╨╕╤Е ╨╝╨╛╨╗╨╡╨║╤Г╨╗╤Л ╨╝╨░╨╗╨╛╨┐╨╛╨╗╤П╤А╨╜╤Л ╨╕ ╨╜╨╡ ╨▓╨╖╨░╨╕╨╝╨╛╨┤╨╡╨╣╤Б╤В╨▓╤Г╤О╤В ╤Б ╨╝╨╛╨╗╨╡╨║╤Г╨╗╨░╨╝╨╕ ╨▓╨╛╨┤╤Л. ╨Ц╨╕╨┤╨║╨╕╨╡ ╨░╨╗╨║╨░╨╜╤Л ╨╗╨╡╨│╨║╨╛ ╤Б╨╝╨╡╤И╨╕╨▓╨░╤О╤В╤Б╤П ╨┤╤А╤Г╨│ ╤Б ╨┤╤А╤Г╨│╨╛╨╝. ╨Ю╨╜╨╕ ╤Е╨╛╤А╨╛╤И╨╛ ╤А╨░╤Б╤В╨▓╨╛╤А╤П╤О╤В╤Б╤П ╨▓ ╨╜╨╡╨┐╨╛╨╗╤П╤А╨╜╤Л╤Е ╨╛╤А╨│╨░╨╜╨╕╤З╨╡╤Б╨║╨╕╤Е ╤А╨░╤Б╤В╨▓╨╛╤А╨╕╤В╨╡╨╗╤П╤Е, ╤В╨░╨║╨╕╤Е, ╨║╨░╨║ ╨▒╨╡╨╜╨╖╨╛╨╗, ╤В╨╡╤В╤А╨░╤Е╨╗╨╛╤А╨╝╨╡╤В╨░╨╜ ╨╕ ╨┤╤А.
╨Я╨╛╨╗╤Г╤З╨╡╨╜╨╕╨╡. ╨Ь╨╡╤В╨░╨╜ ╤И╨╕╤А╨╛╨║╨╛ ╤А╨░╤Б╨┐╤А╨╛╤Б╤В╤А╨░╨╜╨╡╨╜ ╨▓ ╨┐╤А╨╕╤А╨╛╨┤╨╡. ╨Ю╨╜ ╤П╨▓╨╗╤П╨╡╤В╤Б╤П ╨│╨╗╨░╨▓╨╜╨╛╨╣ ╤Б╨╛╤Б╤В╨░╨▓╨╜╨╛╨╣ ╤З╨░╤Б╤В╤М╤О ╨╝╨╜╨╛╨│╨╕╤Е ╨│╨╛╤А╤О╤З╨╕╤Е ╨│╨░╨╖╨╛╨▓ ╨║╨░╨║ ╨┐╤А╨╕╤А╨╛╨┤╨╜╤Л╤Е (90-98%), ╤В╨░╨║ ╨╕ ╨╕╤Б╨║╤Г╤Б╤Б╤В╨▓╨╡╨╜╨╜╤Л╤Е, ╨▓╤Л╨┤╨╡╨╗╤П╤О╤Й╨╕╤Е╤Б╤П ╨┐╤А╨╕ ╤Б╤Г╤Е╨╛╨╣ ╨┐╨╡╤А╨╡╨│╨╛╨╜╨║╨╡ ╨┤╨╡╤А╨╡╨▓╨░, ╤В╨╛╤А╤Д╨░, ╨║╨░╨╝╨╡╨╜╨╜╨╛╨│╨╛ ╤Г╨│╨╗╤П, ╨░ ╤В╨░╨║╨╢╨╡ ╨┐╤А╨╕ ╨║╤А╨╡╨║╨╕╨╜╨│╨╡ ╨╜╨╡╤Д╤В╨╕. ╨Я╤А╨╕╤А╨╛╨┤╨╜╤Л╨╡ ╨│╨░╨╖╤Л, ╨╛╤Б╨╛╨▒╨╡╨╜╨╜╨╛ ╨┐╨╛╨┐╤Г╤В╨╜╤Л╨╡ ╨│╨░╨╖╤Л ╨╜╨╡╤Д╤В╤П╨╜╤Л╤Е ╨╝╨╡╤Б╤В╨╛╤А╨╛╨╢╨┤╨╡╨╜╨╕╨╣, ╨┐╨╛╨╝╨╕╨╝╨╛ ╨╝╨╡╤В╨░╨╜╨░ ╤Б╨╛╨┤╨╡╤А╨╢╨░╤В ╤Н╤В╨░╨╜, ╨┐╤А╨╛╨┐╨░╨╜, ╨▒╤Г╤В╨░╨╜ ╨╕ ╨┐╨╡╨╜╤В╨░╨╜.
╨Ь╨╡╤В╨░╨╜ ╨▓╤Л╨┤╨╡╨╗╤П╨╡╤В╤Б╤П ╤Б╨╛ ╨┤╨╜╨░ ╨▒╨╛╨╗╨╛╤В ╨╕ ╨╕╨╖ ╨║╨░╨╝╨╡╨╜╨╜╨╛╤Г╨│╨╛╨╗╤М╨╜╤Л╤Е ╨┐╨╗╨░╤Б╤В╨╛╨▓ ╨▓ ╤А╤Г╨┤╨╜╨╕╨║╨░╤Е, ╨│╨┤╨╡ ╨╛╨╜ ╨╛╨▒╤А╨░╨╖╤Г╨╡╤В╤Б╤П ╨┐╤А╨╕ ╨╝╨╡╨┤╨╗╨╡╨╜╨╜╨╛╨╝ ╤А╨░╨╖╨╗╨╛╨╢╨╡╨╜╨╕╨╕ ╤А╨░╤Б╤В╨╕╤В╨╡╨╗╤М╨╜╤Л╤Е ╨╛╤Б╤В╨░╤В╨║╨╛╨▓ ╨▒╨╡╨╖ ╨┤╨╛╤Б╤В╤Г╨┐╨░ ╨▓╨╛╨╖╨┤╤Г╤Е╨░. ╨Я╨╛╤Н╤В╨╛╨╝╤Г ╨╝╨╡╤В╨░╨╜ ╤З╨░╤Б╤В╨╛ ╨╜╨░╨╖╤Л╨▓╨░╤О╤В ╨▒╨╛╨╗╨╛╤В╨╜╤Л╨╝ ╨│╨░╨╖╨╛╨╝ ╨╕╨╗╨╕ ╤А╤Г╨┤╨╜╨╕╤З╨╜╤Л╨╝ ╨│╨░╨╖╨╛╨╝.
1. ╨Я╨╛╨╗╤Г╤З╨╡╨╜╨╕╨╡ ╨╕╨╖ ╨╜╨╡╨╜╨░╤Б╤Л╤Й╨╡╨╜╨╜╤Л╤Е ╤Г╨│╨╗╨╡╨▓╨╛╨┤╨╛╤А╨╛╨┤╨╛╨▓.
╨Т╨╖╨░╨╕╨╝╨╛╨┤╨╡╨╣╤Б╤В╨▓╨╕╨╡ ╨░╨╗╨║╨░╨╜╨╛╨▓ ╤Б ╨▓╨╛╨┤╨╛╤А╨╛╨┤╨╛╨╝ ╨┐╤А╨╛╨╕╤Б╤Е╨╛╨┤╨╕╤В ╨▓ ╨┐╤А╨╕╤Б╤Г╤В╤Б╤В╨▓╨╕╨╕ ╨╝╨╡╤В╨░╨╗╨╗╨╕╤З╨╡╤Б╨║╨╕╤Е ╨║╨░╤В╨░╨╗╨╕╨╖╨░╤В╨╛╤А╨╛╨▓ (Ni, Pd) ╨┐╤А╨╕ ╨╜╨░╨│╤А╨╡╨▓╨░╨╜╨╕╨╕:
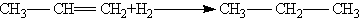
2. ╨Я╨╛╨╗╤Г╤З╨╡╨╜╨╕╨╡ ╨╕╨╖ ╨│╨░╨╗╨╛╨│╨╡╨╜╨╛╨┐╤А╨╛╨╕╨╖╨▓╨╛╨┤╨╜╤Л╤Е.
╨Я╤А╨╕ ╨╜╨░╨│╤А╨╡╨▓╨░╨╜╨╕╨╕ ╨╝╨╛╨╜╨╛╨│╨░╨╗╨╛╨│╨╡╨╜╨╛╨╖╨░╨╝╨╡╤Й╨╡╨╜╨╜╤Л╤Е ╨░╨╗╨║╨░╨╜╨╛╨▓ ╤Б ╨╝╨╡╤В╨░╨╗╨╗╨╕╤З╨╡╤Б╨║╨╕╨╝ ╨╜╨░╤В╤А╨╕╨╡╨╝ ╨┐╨╛╨╗╤Г╤З╨░╤О╤В ╨░╨╗╨║╨░╨╜╤Л ╤Б ╤Г╨┤╨▓╨╛╨╡╨╜╨╜╤Л╨╝ ╤З╨╕╤Б╨╗╨╛╨╝ ╨░╤В╨╛╨╝╨╛╨▓ ╤Г╨│╨╗╨╡╤А╨╛╨┤╨░ (╤А╨╡╨░╨║╤Ж╨╕╤П ╨Т╤О╤А╤Ж╨░):
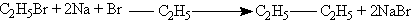
╨Я╨╛╨┤╨╛╨▒╨╜╤Г╤О ╤А╨╡╨░╨║╤Ж╨╕╤О ╨╜╨╡ ╨┐╤А╨╛╨▓╨╛╨┤╤П╤В ╤Б ╨┤╨▓╤Г╨╝╤П ╤А╨░╨╖╨╜╤Л╨╝╨╕ ╨│╨░╨╗╨╛╨│╨╡╨╜╨╛╨╖╨░╨╝╨╡╤Й╨╡╨╜╨╜╤Л╨╝╨╕ ╨░╨╗╨║╨░╨╜╨░╨╝╨╕, ╨┐╨╛╤Б╨║╨╛╨╗╤М╨║╤Г ╨┐╤А╨╕ ╤Н╤В╨╛╨╝ ╨┐╨╛╨╗╤Г╤З╨░╨╡╤В╤Б╤П ╤Б╨╝╨╡╤Б╤М ╤В╤А╨╡╤Е ╤А╨░╨╖╨╗╨╕╤З╨╜╤Л╤Е ╨░╨╗╨║╨░╨╜╨╛╨▓.
3. ╨Я╨╛╨╗╤Г╤З╨╡╨╜╨╕╨╡ ╨╕╨╖ ╤Б╨╛╨╗╨╡╨╣ ╨║╨░╤А╨▒╨╛╨╜╨╛╨▓╤Л╤Е ╨║╨╕╤Б╨╗╨╛╤В.
╨Я╤А╨╕ ╤Б╨┐╨╗╨░╨▓╨╗╨╡╨╜╨╕╨╕ ╨▒╨╡╨╖╨▓╨╛╨┤╨╜╤Л╤Е ╤Б╨╛╨╗╨╡╨╣ ╨║╨░╤А╨▒╨╛╨╜╨╛╨▓╤Л╤Е ╨║╨╕╤Б╨╗╨╛╤В ╤Б ╤Й╨╡╨╗╨╛╤З╨░╨╝╨╕ ╨┐╨╛╨╗╤Г╤З╨░╤О╤В╤Б╤П ╨░╨╗╨║╨░╨╜╤Л, ╤Б╨╛╨┤╨╡╤А╨╢╨░╤Й╨╕╨╡ ╨╜╨░ ╨╛╨┤╨╕╨╜ ╨░╤В╨╛╨╝ ╤Г╨│╨╗╨╡╤А╨╛╨┤╨░ ╨╝╨╡╨╜╤М╤И╨╡ ╨┐╨╛ ╤Б╤А╨░╨▓╨╜╨╡╨╜╨╕╤О ╤Б ╤Г╨│╨╗╨╡╤А╨╛╨┤╨╜╨╛╨╣ ╤Ж╨╡╨┐╤М╤О ╨╕╤Б╤Е╨╛╨┤╨╜╤Л╤Е ╨║╨░╤А╨▒╨╛╨╜╨╛╨▓╤Л╤Е ╨║╨╕╤Б╨╗╨╛╤В:
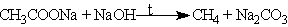
4. ╨Я╨╛╨╗╤Г╤З╨╡╨╜╨╕╨╡ ╨╝╨╡╤В╨░╨╜╨░.
╨Т ╤Н╨╗╨╡╨║╤В╤А╨╕╤З╨╡╤Б╨║╨╛╨╣ ╨┤╤Г╨│╨╡, ╨│╨╛╤А╤П╤Й╨╡╨╣ ╨▓ ╨░╤В╨╝╨╛╤Б╤Д╨╡╤А╨╡ ╨▓╨╛╨┤╨╛╤А╨╛╨┤╨░, ╨╛╨▒╤А╨░╨╖╤Г╨╡╤В╤Б╤П ╨╖╨╜╨░╤З╨╕╤В╨╡╨╗╤М╨╜╨╛╨╡ ╨║╨╛╨╗╨╕╤З╨╡╤Б╤В╨▓╨╛ ╨╝╨╡╤В╨░╨╜╨░:
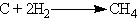
╨в╨░╨║╨░╤П ╨╢╨╡ ╤А╨╡╨░╨║╤Ж╨╕╤П ╨╕╨┤╨╡╤В ╨┐╤А╨╕ ╨╜╨░╨│╤А╨╡╨▓╨░╨╜╨╕╨╕ ╤Г╨│╨╗╨╡╤А╨╛╨┤╨░ ╨▓ ╨░╤В╨╝╨╛╤Б╤Д╨╡╤А╨╡ ╨▓╨╛╨┤╨╛╤А╨╛╨┤╨░ ╨┤╨╛ 400тАФ500 ┬░╨б ╨┐╤А╨╕ ╨┐╨╛╨▓╤Л╤И╨╡╨╜╨╜╨╛╨╝ ╨┤╨░╨▓╨╗╨╡╨╜╨╕╨╕ ╨▓ ╨┐╤А╨╕╤Б╤Г╤В╤Б╤В╨▓╨╕╨╕ ╨║╨░╤В╨░╨╗╨╕╨╖╨░╤В╨╛╤А╨░.
╨Т ╨╗╨░╨▒╨╛╤А╨░╤В╨╛╤А╨╜╤Л╤Е ╤Г╤Б╨╗╨╛╨▓╨╕╤П╤Е ╨╝╨╡╤В╨░╨╜ ╤З╨░╤Б╤В╨╛ ╨┐╨╛╨╗╤Г╤З╨░╤О╤В ╨╕╨╖ ╨║╨░╤А╨▒╨╕╨┤╨░ ╨░╨╗╤О╨╝╨╕╨╜╨╕╤П:
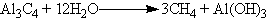
╨е╨╕╨╝╨╕╤З╨╡╤Б╨║╨╕╨╡ ╤Б╨▓╨╛╨╣╤Б╤В╨▓╨░. ╨Т ╨╛╨▒╤Л╤З╨╜╤Л╤Е ╤Г╤Б╨╗╨╛╨▓╨╕╤П╤Е ╨░╨╗╨║╨░╨╜╤Л ╤Е╨╕╨╝╨╕╤З╨╡╤Б╨║╨╕ ╨╕╨╜╨╡╤А╤В╨╜╤Л. ╨Ю╨╜╨╕ ╤Г╤Б╤В╨╛╨╣╤З╨╕╨▓╤Л ╨║ ╨┤╨╡╨╣╤Б╤В╨▓╨╕╤О ╨╝╨╜╨╛╨│╨╕╤Е ╤А╨╡╨░╨│╨╡╨╜╤В╨╛╨▓: ╨╜╨╡ ╨▓╨╖╨░╨╕╨╝╨╛╨┤╨╡╨╣╤Б╤В╨▓╤Г╤О╤В ╤Б ╨║╨╛╨╜╤Ж╨╡╨╜╤В╤А╨╕╤А╨╛╨▓╨░╨╜╨╜╤Л╨╝╨╕ ╤Б╨╡╤А╨╜╨╛╨╣ ╨╕ ╨░╨╖╨╛╤В╨╜╨╛╨╣ ╨║╨╕╤Б╨╗╨╛╤В╨░╨╝╨╕, ╤Б ╨║╨╛╨╜╤Ж╨╡╨╜╤В╤А╨╕╤А╨╛╨▓╨░╨╜╨╜╤Л╨╝╨╕ ╨╕ ╤А╨░╤Б╨┐╨╗╨░╨▓╨╗╨╡╨╜╨╜╤Л╨╝╨╕ ╤Й╨╡╨╗╨╛╤З╨░╨╝╨╕, ╨╜╨╡ ╨╛╨║╨╕╤Б╨╗╤П╤О╤В╤Б╤П ╤Б╨╕╨╗╤М╨╜╤Л╨╝╨╕ ╨╛╨║╨╕╤Б╨╗╨╕╤В╨╡╨╗╤П╨╝╨╕ тАФ ╨┐╨╡╤А╨╝╨░╨╜╨│╨░╨╜╨░╤В╨╛╨╝ ╨║╨░╨╗╨╕╤П ╨Ъ╨╝n╨Ю4 ╨╕ ╤В. ╨┐.
╨е╨╕╨╝╨╕╤З╨╡╤Б╨║╨░╤П ╤Г╤Б╤В╨╛╨╣╤З╨╕╨▓╨╛╤Б╤В╤М ╨░╨╗╨║╨░╨╜╨╛╨▓ ╨╛╨▒╤К╤П╤Б╨╜╤П╨╡╤В╤Б╤П ╨▓╤Л╤Б╨╛╨║╨╛╨╣ ╨┐╤А╨╛╤З╨╜╨╛╤Б╤В╤М╤О s -╤Б╨▓╤П╨╖╨╡╨╣ ╨бтАФ╨б ╨╕ ╨бтАФ╨Э, ╨░ ╤В╨░╨║╨╢╨╡ ╨╕╤Е ╨╜╨╡╨┐╨╛╨╗╤П╤А╨╜╨╛╤Б╤В╤М╤О. ╨Э╨╡╨┐╨╛╨╗╤П╤А╨╜╤Л╨╡ ╤Б╨▓╤П╨╖╨╕ ╨бтАФ╨б ╨╕ ╨бтАФ╨Э ╨▓ ╨░╨╗╨║╨░╨╜╨░╤Е ╨╜╨╡ ╤Б╨║╨╗╨╛╨╜╨╜╤Л ╨║ ╨╕╨╛╨╜╨╜╨╛╨╝╤Г ╤А╨░╨╖╤А╤Л╨▓╤Г, ╨╜╨╛ ╤Б╨┐╨╛╤Б╨╛╨▒╨╜╤Л ╤А╨░╤Б╤Й╨╡╨┐╨╗╤П╤В╤М╤Б╤П ╨│╨╛╨╝╨╛╨╗╨╕╤В╨╕╤З╨╡╤Б╨║╨╕ ╨┐╨╛╨┤ ╨┤╨╡╨╣╤Б╤В╨▓╨╕╨╡╨╝ ╨░╨║╤В╨╕╨▓╨╜╤Л╤Е ╤Б╨▓╨╛╨▒╨╛╨┤╨╜╤Л╤Е ╤А╨░╨┤╨╕╨║╨░╨╗╨╛╨▓. ╨Я╨╛╤Н╤В╨╛╨╝╤Г ╨┤╨╗╤П ╨░╨╗╨║╨░╨╜╨╛╨▓ ╤Е╨░╤А╨░╨║╤В╨╡╤А╨╜╤Л, ╤А╨░╨┤╨╕╨║╨░╨╗╤М╨╜╤Л╨╡ ╤А╨╡╨░╨║╤Ж╨╕╨╕, ╨▓ ╤А╨╡╨╖╤Г╨╗╤М╤В╨░╤В╨╡ ╨║╨╛╤В╨╛╤А╤Л╤Е ╨┐╨╛╨╗╤Г╤З╨░╤О╤В╤Б╤П ╤Б╨╛╨╡╨┤╨╕╨╜╨╡╨╜╨╕╤П, ╨│╨┤╨╡ ╨░╤В╨╛╨╝╤Л ╨▓╨╛╨┤╨╛╤А╨╛╨┤╨░ ╨╖╨░╨╝╨╡╤Й╨╡╨╜╤Л ╨╜╨░ ╨┤╤А╤Г╨│╨╕╨╡ ╨░╤В╨╛╨╝╤Л ╨╕╨╗╨╕ ╨│╤А╤Г╨┐╨┐╤Л ╨░╤В╨╛╨╝╨╛╨▓. A╨╗╨║╨░╨╜╤Л ╨▓╤Б╤В╤Г╨┐╨░╤О╤В ╨▓ ╤А╨╡╨░╨║╤Ж╨╕╨╕, ╨┐╤А╨╛╤В╨╡╨║╨░╤О╤Й╨╕╨╡ ╨┐╨╛ ╨╝╨╡╤Е╨░╨╜╨╕╨╖╨╝╤Г ╤А╨░╨┤╨╕╨║╨░╨╗╤М╨╜╨╛╨│╨╛ ╨╖╨░╨╝╨╡╤Й╨╡╨╜╨╕╤П, ╨╛╨▒╨╛╨╖╨╜╨░╤З╨░╨╡╨╝╨╛╨│╨╛ ╤Б╨╕╨╝╨▓╨╛╨╗╨╛╨╝ SR (╨╛╤В ╨░╨╜╨│╨╗.substitution radicalic). ╨Я╨╛ ╤Н╤В╨╛╨╝╤Г ╨╝╨╡╤Е╨░╨╜╨╕╨╖╨╝╤Г ╨╗╨╡╨│╤З╨╡ ╨▓╤Б╨╡╨│╨╛ ╨╖╨░╨╝╨╡╤Й╨░╤О╤В╤Б╤П ╨░╤В╨╛╨╝╤Л ╨▓╨╛╨┤╨╛╤А╨╛╨┤╨░ ╤Г ╤В╤А╨╡╤В╨╕╤З╨╜╤Л╤Е, ╨╖╨░╤В╨╡╨╝ ╤Г ╨▓╤В╨╛╤А╨╕╤З╨╜╤Л╤Е ╨╕ ╨┐╨╡╤А╨▓╨╕╤З╨╜╤Л╤Е ╨░╤В╨╛╨╝╨╛╨▓ ╤Г╨│╨╗╨╡╤А╨╛╨┤╨░.
╨У╨░╨╗╨╛╨│╨╡╨╜╨╕╤А╨╛╨▓╨░╨╜╨╕╨╡.
╨Я╤А╨╕ ╨▓╨╖╨░╨╕╨╝╨╛╨┤╨╡╨╣╤Б╤В╨▓╨╕╨╕ ╨░╨╗╨║╨░╨╜╨╛╨▓ ╤Б ╨│╨░╨╗╨╛╨│╨╡╨╜╨░╨╝╨╕ (╤Е╨╗╨╛╤А╨╛╨╝ ╨╕ ╨▒╤А╨╛╨╝╨╛╨╝) ╨┐╨╛╨┤ ╨┤╨╡╨╣╤Б╤В╨▓╨╕╨╡╨╝ ╨г╨д-╨╕╨╖╨╗╤Г╤З╨╡╨╜╨╕╤П ╨╕╨╗╨╕ ╨▓╤Л╤Б╨╛╨║╨╛╨╣ ╤В╨╡╨╝╨┐╨╡╤А╨░╤В╤Г╤А╤Л ╨╛╨▒╤А╨░╨╖╤Г╨╡╤В╤Б╤П ╤Б╨╝╨╡╤Б╤М ╨┐╤А╨╛╨┤╤Г╨║╤В╨╛╨▓ ╨╛╤В ╨╝╨╛╨╜╨╛- ╨┤╨╛ ╨┐╨╛╨╗╨╕╨│╨░╨╗╨╛╨│╨╡╨╜╨╛╨╖╨░╨╝╨╡╤Й╨╡╨╜╨╜╤Л╤Е ╨░╨╗╨║╨░╨╜╨╛╨▓. ╨Ю╨▒╤Й╨░╤П ╤Б╤Е╨╡╨╝╨░ ╤Н╤В╨╛╨╣ ╤А╨╡╨░╨║╤Ж╨╕╨╕ ╨┐╨╛╨║╨░╨╖╨░╨╜╨░ ╨╜╨░ ╨┐╤А╨╕╨╝╨╡╤А╨╡ ╨╝╨╡╤В╨░╨╜╨░:
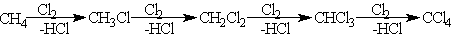
╨Э╨╕╤В╤А╨╛╨▓╨░╨╜╨╕╨╡ (╤А╨╡╨░╨║╤Ж╨╕╤П ╨Ъ╨╛╨╜╨╛╨▓╨░╨╗╨╛╨▓╨░).
╨Я╤А╨╕ ╨┤╨╡╨╣╤Б╤В╨▓╨╕╨╕ ╤А╨░╨╖╨▒╨░╨▓╨╗╨╡╨╜╨╜╨╛╨╣ ╨░╨╖╨╛╤В╨╜╨╛╨╣ ╨║╨╕╤Б╨╗╨╛╤В╤Л ╨╜╨░ ╨░╨╗╨║╨░╨╜╤Л ╨┐╤А╨╕ 140 "╨б ╨╕ ╨╜╨╡╨▒╨╛╨╗╤М╤И╨╛╨╝ ╨┤╨░╨▓╨╗╨╡╨╜╨╕╨╕ ╨┐╤А╨╛╤В╨╡╨║╨░╨╡╤В ╤А╨░╨┤╨╕╨║╨░╨╗╤М╨╜╨░╤П ╤А╨╡╨░╨║╤Ж╨╕╤П:
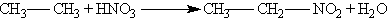
╨Ш╨╖╨╛╨╝╨╡╤А╨╕╨╖╨░╤Ж╨╕╤П.
╨Э╨╛╤А╨╝╨░╨╗╤М╨╜╤Л╨╡ ╨░╨╗╨║╨░╨╜╤Л ╨┐╤А╨╕ ╨╛╨┐╤А╨╡╨┤╨╡╨╗╨╡╨╜╨╜╤Л╤Е ╤Г╤Б╨╗╨╛╨▓╨╕╤П╤Е ╨╝╨╛╨│╤Г╤В ╨┐╤А╨╡╨▓╤А╨░╤Й╨░╤В╤М╤Б╤П ╨▓ ╨░╨╗╨║╨░╨╜╤Л ╤Б ╤А╨░╨╖╨▓╨╡╤В╨▓╨╗╨╡╨╜╨╜╨╛╨╣ ╤Ж╨╡╨┐╤М╤О:
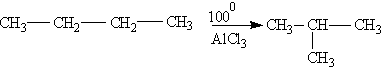
╨Ю╨║╨╕╤Б╨╗╨╡╨╜╨╕╨╡.
╨Я╤А╨╕ ╨╝╤П╨│╨║╨╛╨╝ ╨╛╨║╨╕╤Б╨╗╨╡╨╜╨╕╨╕ ╨╝╨╡╤В╨░╨╜╨░ ╨║╨╕╤Б╨╗╨╛╤А╨╛╨┤╨╛╨╝ ╨▓╨╛╨╖╨┤╤Г╤Е╨░ ╨▓ ╨┐╤А╨╕╤Б╤Г╤В╤Б╤В╨▓╨╕╨╕ ╤А╨░╨╖╨╗╨╕╤З╨╜╤Л╤Е ╨║╨░╤В╨░╨╗╨╕╨╖╨░╤В╨╛╤А╨╛╨▓ ╨╝╨╛╨│╤Г╤В ╨▒╤Л╤В╤М ╨┐╨╛╨╗╤Г╤З╨╡╨╜╤Л ╨╝╨╡╤В╨╕╨╗╨╛╨▓╤Л╨╣ ╤Б╨┐╨╕╤А╤В, ╤Д╨╛╤А╨╝╨░╨╗╤М╨┤╨╡╨│╨╕╨┤, ╨╝╤Г╤А╨░╨▓╤М╨╕╨╜╨░╤П ╨║╨╕╤Б╨╗╨╛╤В╨░:
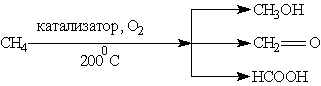
╨Э╨░ ╨▓╨╛╨╖╨┤╤Г╤Е╨╡ ╨░╨╗╨║╨░╨╜╤Л ╤Б╨│╨╛╤А╨░╤О╤В ╨┤╨╛ ╨б╨Ю2 ╨╕ ╨Э2╨Ю.
╨Я╤А╨╕╨╝╨╡╨╜╨╡╨╜╨╕╨╡ ╨░╨╗╨║╨░╨╜╨╛╨▓. ╨Ю╨╜╨╛ ╨▓╨╡╤Б╤М╨╝╨░ ╤А╨░╨╖╨╜╨╛╨╛╨▒╤А╨░╨╖╨╜╨╛. ╨С╨╗╨░╨│╨╛╨┤╨░╤А╤П ╨▒╨╛╨╗╤М╤И╨╛╨╣ ╤В╨╡╨┐╨╗╨╛╤В╨▓╨╛╤А╨╜╨╛╨╣ ╤Б╨┐╨╛╤Б╨╛╨▒╨╜╨╛╤Б╤В╨╕ ╨╝╨╡╤В╨░╨╜ ╨▓ ╨▒╨╛╨╗╤М╤И╨╕╤Е ╨║╨╛╨╗╨╕╤З╨╡╤Б╤В╨▓╨░╤Е ╤А╨░╤Б╤Е╨╛╨┤╤Г╨╡╤В╤Б╤П ╨▓ ╨║╨░╤З╨╡╤Б╤В╨▓╨╡ ╤В╨╛╨┐╨╗╨╕╨▓╨░ (╨▓ ╨▒╤Л╤В╤Г тАФ ╨▒╤Л╤В╨╛╨▓╨╛╨╣ ╨│╨░╨╖ ╨╕ ╨▓ ╨┐╤А╨╛╨╝╤Л╤И╨╗╨╡╨╜╨╜╨╛╤Б╤В╨╕). ╨и╨╕╤А╨╛╨║╨╛ ╨┐╤А╨╕╨╝╨╡╨╜╤П╤О╤В╤Б╤П ╨┐╨╛╨╗╤Г╤З╨░╨╡╨╝╤Л╨╡ ╨╕╨╖ ╨╜╨╡╨│╨╛ ╨▓╨╡╤Й╨╡╤Б╤В╨▓╨░: ╨▓╨╛╨┤╨╛╤А╨╛╨┤, ╨░╤Ж╨╡╤В╨╕╨╗╨╡╨╜, ╤Б╨░╨╢╨░. ╨Ю╨╜ ╤Б╨╗╤Г╨╢╨╕╤В ╨╕╤Б╤Е╨╛╨┤╨╜╤Л╨╝ ╤Б╤Л╤А╤М╨╡╨╝ ╨┤╨╗╤П ╨┐╨╛╨╗╤Г╤З╨╡╨╜╨╕╤П ╤Д╨╛╤А╨╝╨░╨╗╤М╨┤╨╡╨│╨╕╨┤╨░, ╨╝╨╡╤В╨╕╨╗╨╛╨▓╨╛╨│╨╛ ╤Б╨┐╨╕╤А╤В╨░, ╨░ ╤В╨░╨║╨╢╨╡ ╤А╨░╨╖╨╗╨╕╤З╨╜╤Л╤Е ╤Б╨╕╨╜╤В╨╡╤В╨╕╤З╨╡╤Б╨║╨╕╤Е ╨┐╤А╨╛╨┤╤Г╨║╤В╨╛╨▓.
╨С╨╛╨╗╤М╤И╨╛╨╡ ╨┐╤А╨╛╨╝╤Л╤И╨╗╨╡╨╜╨╜╨╛╨╡ ╨╖╨╜╨░╤З╨╡╨╜╨╕╨╡ ╨╕╨╝╨╡╨╡╤В ╨╛╨║╨╕╤Б╨╗╨╡╨╜╨╕╨╡ ╨▓╤Л╤Б╤И╨╕╤Е ╨┐╤А╨╡╨┤╨╡╨╗╤М╨╜╤Л╤Е ╤Г╨│╨╗╨╡╨▓╨╛╨┤╨╛╤А╨╛╨┤╨╛╨▓ тАФ ╨┐╨░╤А╨░╤Д╨╕╨╜╨╛╨▓ ╤Б ╤З╨╕╤Б╨╗╨╛╨╝ ╤Г╨│╨╗╨╡╤А╨╛╨┤╨╜╤Л╤Е ╨░╤В╨╛╨╝╨╛╨▓ 20-25. ╨н╤В╨╕╨╝ ╨┐╤Г╤В╨╡╨╝ ╨┐╨╛╨╗╤Г╤З╨░╤О╤В ╤Б╨╕╨╜╤В╨╡╤В╨╕╤З╨╡╤Б╨║╨╕╨╡ ╨╢╨╕╤А╨╜╤Л╨╡ ╨║╨╕╤Б╨╗╨╛╤В╤Л ╤Б ╤А╨░╨╖╨╗╨╕╤З╨╜╨╛╨╣ ╨┤╨╗╨╕╨╜╨╛╨╣ ╤Ж╨╡╨┐╨╕, ╨║╨╛╤В╨╛╤А╤Л╨╡ ╨╕╤Б╨┐╨╛╨╗╤М╨╖╤Г╤О╤В╤Б╤П ╨┤╨╗╤П ╨┐╤А╨╛╨╕╨╖╨▓╨╛╨┤╤Б╤В╨▓╨░ ╨╝╤Л╨╗, ╤А╨░╨╖╨╗╨╕╤З╨╜╤Л╤Е ╨╝╨╛╤О╤Й╨╕╤Е ╤Б╤А╨╡╨┤╤Б╤В╨▓, ╤Б╨╝╨░╨╖╨╛╤З╨╜╤Л╤Е ╨╝╨░╤В╨╡╤А╨╕╨░╨╗╨╛╨▓, ╨╗╨░╨║╨╛╨▓ ╨╕ ╤Н╨╝╨░╨╗╨╡╨╣.
╨Ц╨╕╨┤╨║╨╕╨╡ ╤Г╨│╨╗╨╡╨▓╨╛╨┤╨╛╤А╨╛╨┤╤Л ╨╕╤Б╨┐╨╛╨╗╤М╨╖╤Г╤О╤В╤Б╤П ╨║╨░╨║ ╨│╨╛╤А╤О╤З╨╡╨╡ (╨╛╨╜╨╕ ╨▓╤Е╨╛╨┤╤П╤В ╨▓ ╤Б╨╛╤Б╤В╨░╨▓ ╨▒╨╡╨╜╨╖╨╕╨╜╨░ ╨╕ ╨║╨╡╤А╨╛╤Б╨╕╨╜╨░). ╨Р╨╗╨║╨░╨╜╤Л ╤И╨╕╤А╨╛╨║╨╛ ╨╕╤Б╨┐╨╛╨╗╤М╨╖╤Г╤О╤В╤Б╤П ╨▓ ╨╛╤А╨│╨░╨╜╨╕╤З╨╡╤Б╨║╨╛╨╝ ╤Б╨╕╨╜╤В╨╡╨╖╨╡.
╨ж╨╕╨║╨╗╨╛╨░╨╗╨║╨░╨╜╤Л. ╨Ю╨▒╤Й╨░╤П ╤Д╨╛╤А╨╝╤Г╨╗╨░ ╨│╨╛╨╝╨╛╨╗╨╛╨│╨╕╤З╨╡╤Б╨║╨╛╨│╨╛ ╤А╤П╨┤╨░ ╤Ж╨╕╨║╨╗╨╛╨░╨╗╨║╨░╨╜╨╛╨▓ ╨б2╨Э2n. ╨в╨╛╤З╨╜╨╛ ╤В╨░╨║╨╛╨╣ ╨╢╨╡ ╤Д╨╛╤А╨╝╤Г╨╗╨╛╨╣ ╨╛╨┐╨╕╤Б╤Л╨▓╨░╨╡╤В╤Б╤П ╨│╨╛╨╝╨╛╨╗╨╛╨│╨╕╤З╨╡╤Б╨║╨╕╨╣ ╤А╤П╨┤ ╨░╨╗╨║╨╡╨╜╨╛╨▓, ╨╕╨╖ ╤З╨╡╨│╨╛ ╤Б╨╗╨╡╨┤╤Г╨╡╤В, ╤З╤В╨╛ ╨║╨░╨╢╨┤╨╛╨╝╤Г ╤Ж╨╕╨║╨╗╨╛╨░╨╗╨║╨░╨╜╤Г ╨╕╨╖╨╛╨╝╨╡╤А╨╡╨╜ ╤Б╨╛╨╛╤В╨▓╨╡╤В╤Б╤В╨▓╤Г╤О╤Й╨╕╨╣ ╨░╨╗╨║╨╡╨╜ тАФ ╤Н╤В╨╛ ╨┐╤А╨╕╨╝╨╡ ╤В╨░╨║ ╨╜╨░╨╖╤Л╨▓╨░╨╡╨╝╨╛╨╣ тАЬ╨╝╨╡╨╢╨║╨╗╨░╤Б╤Б╨╛╨▓╨╛╨╣тАЭ ╨╕╨╖╨╛╨╝╨╡╤А╨╕╨╕.
╨Я╨╛ ╤А╨░╨╖╨╝╨╡╤А╤Г ╤Ж╨╕╨║╨╗╨░ ╤Ж╨╕╨║╨╗╨╛╨░╨╗╨║╨░╨╜╤Л ╨┤╨╡╨╗╤П╤В╤Б╤П ╨╜╨░ ╤А╤П╨┤ ╨│╤А╤Г╨┐╨┐, ╨╕╨╖ ╨║╨╛╤В╨╛╤А╤Л╤Е ╨╝╤Л ╤А╨░╤Б╤Б╨╝╨╛╤В╤А╨╕╨╝ ╨╝╨░╨╗╤Л╨╡ (╨б3, ╨б4) ╨╕ ╨╛╨▒╤Л╤З╨╜╤Л╨╡ (╨б5тАФ╨б7) ╤Ж╨╕╨║╨╗╤Л.
╨Э╨░╨╖╨▓╨░╨╜╨╕╤П ╤Ж╨╕╨║╨╗╨╛╨░╨╗╨║╨░╨╜╨╛╨▓ ╤Б╤В╤А╨╛╤П╤В╤Б╤П ╨┐╤Г╤В╨╡╨╝ ╨┤╨╛╨▒╨░╨▓╨╗╨╡╨╜╨╕╤П ╨┐╤А╨╕╤Б╤В╨░╨▓╨║╨╕ ╤Ж╨╕╨║╨╗╨╛- ╨║ ╨╜╨░╨╖╨▓╨░╨╜╨╕╤О ╨░╨╗╨║╨░╨╜╨░ ╤Б ╤Б╨╛╨╛╤В╨▓╨╡╤В╤Б╤В╨▓╤Г╤О╤Й╨╕╨╝ ╤З╨╕╤Б╨╗╨╛╨╝ ╨░╤В╨╛╨╝╨╛╨▓ ╤Г╨│╨╗╨╡╤А╨╛╨┤╨░. ╨Э╤Г╨╝╨╡╤А╨░╤Ж╨╕╤О ╨▓ ╤Ж╨╕╨║╨╗╨╡ ╨┐╤А╨╛╨╕╨╖╨▓╨╛╨┤╤П╤В ╤В╨░╨║╨╕╨╝ ╨╛╨▒╤А╨░╨╖╨╛╨╝, ╤З╤В╨╛╨▒╤Л ╨╖╨░╨╝╨╡╤Б╤В╨╕╤В╨╡╨╗╨╕ ╨┐╨╛╨╗╤Г╤З╨╕╨╗╨╕ ╨╜╨░╨╕╨╝╨╡╨╜╤М╤И╨╕╨╡ ╨╜╨╛╨╝╨╡╤А╨░.
╨б╤В╤А╤Г╨║╤В╤Г╤А╨╜╤Л╨╡ ╤Д╨╛╤А╨╝╤Г╨╗╤Л ╤Ж╨╕╨║╨╗╨╛╨░╨╗╨║╨░╨╜╨╛╨▓ ╨╛╨▒╤Л╤З╨╜╨╛ ╨╖╨░╨┐╨╕╤Б╤Л╨▓╨░╤О╤В ╨▓ ╤Б╨╛╨║╤А╨░╤Й╨╡╨╜╨╜╨╛╨╝ ╨▓╨╕╨┤╨╡, ╨╕╤Б╨┐╨╛╨╗╤М╨╖╤Г╤П ╨│╨╡╨╛╨╝╨╡╤В╤А╨╕╤З╨╡╤Б╨║╤Г╤О ╤Д╨╛╤А╨╝╤Г ╤Ж╨╕╨║╨╗╨░ ╨╕ ╨╛╨┐╤Г╤Б╨║╨░╤П ╤Б╨╕╨╝╨▓╨╛╨╗╤Л ╨░╤В╨╛╨╝╨╛╨▓ ╤Г╨│╨╗╨╡╤А╨╛╨┤╨░ ╨╕ ╨▓╨╛╨┤╨╛╤А╨╛╨┤╨░.
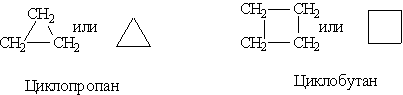
╨б╤В╤А╤Г╨║╤В╤Г╤А╨╜╨░╤П ╨╕╨╖╨╛╨╝╨╡╤А╨╕╤П ╤Ж╨╕╨║╨╗╨╛╨░╨╗╨║╨░╨╜╨╛╨▓ ╨╛╨▒╤Г╤Б╨╗╨╛╨▓╨╗╨╡╨╜╨░ ╤А╨░╨╖╨╝╨╡╤А╨╛╨╝ ╤Ж╨╕╨║╨╗╨░ (╨╜╨░╨┐╤А╨╕╨╝╨╡╤А, ╤Ж╨╕╨║╨╗╨╛╨▒╤Г╤В╨░╨╜ ╨╕ ╨╝╨╡╤В╨╕╨╗╤Ж╨╕╨║╨╗╨╛-╨┐╤А╨╛╨┐╨░╨╜ тАФ ╨╕╨╖╨╛╨╝╨╡╤А╤Л) ╨╕ ╨┐╨╛╨╗╨╛╨╢╨╡╨╜╨╕╨╡╨╝ ╨╖╨░╨╝╨╡╤Б╤В╨╕╤В╨╡╨╗╨╡╨╣ ╨▓ ╤Ж╨╕╨║╨╗╨╡ (╨╜╨░╨┐╤А╨╕╨╝╨╡╤А, 1,1- ╨╕ 1,2-╨┤╨╕╨╝╨╡╤В╨╕╨╗╨▒╤Г╤В╨░╨╜).
╨Ф╨╗╤П ╤Ж╨╕╨║╨╗╨╛╨░╨╗╨║╨░╨╜╨╛╨▓ ╤Е╨░╤А╨░╨║╤В╨╡╤А╨╡╨╜ ╨╡╤Й╨╡ ╨╛╨┤╨╕╨╜ ╨▓╨╕╨┤ ╨╕╨╖╨╛╨╝╨╡╤А╨╕╨╕ тАФ ╨┐╤А╨╛╤Б╤В╤А╨░╨╜╤Б╤В╨▓╨╡╨╜╨╜╨░╤П ╨╕╨╖╨╛╨╝╨╡╤А╨╕╤П, ╤Б╨▓╤П╨╖╨░╨╜╨╜╨░╤П ╤Б ╤А╨░╨╖╨╗╨╕╤З╨╜╤Л╨╝ ╤А╨░╤Б╨┐╨╛╨╗╨╛╨╢╨╡╨╜╨╕╨╡╨╝ ╨╖╨░╨╝╨╡╤Б╤В╨╕╤В╨╡╨╗╨╡╨╣ ╨╛╤В╨╜╨╛╤Б╨╕╤В╨╡╨╗╤М╨╜╨╛ ╨┐╨╗╨╛╤Б╨║╨╛╤Б╤В╨╕ ╤Ж╨╕╨║╨╗╨░. ╨Я╤А╨╕ ╨╕╤Е ╤А╨░╤Б╨┐╨╛╨╗╨╛╨╢╨╡╨╜╨╕╨╕ ╨┐╨╛ ╨╛╨┤╨╜╤Г ╤Б╤В╨╛╤А╨╛╨╜╤Г ╨╛╤В ╨┐╨╗╨╛╤Б╨║╨╛╤Б╤В╨╕ ╤Ж╨╕╨║╨╗╨░ ╨┐╨╛╨╗╤Г╤З╨░╨╡╤В╤Б╤П ╤Ж╨╕╤Б-╨╕╨╖╨╛╨╝╨╡╤А, ╨┐╨╛ ╤А╨░╨╖╨╜╤Л╨╡ ╤Б╤В╨╛╤А╨╛╨╜╤Л тАФ ╤В╤А╨░╨╜╤Б-╨╕╨╖╨╛╨╝╨╡╤А.
╨д╨╕╨╖╨╕╤З╨╡╤Б╨║╨╕╨╡ ╤Б╨▓╨╛╨╣╤Б╤В╨▓╨░. ╨Я╨╡╤А╨▓╤Л╨╡ ╨┤╨▓╨░ ╤З╨╗╨╡╨╜╨░ ╤Н╤В╨╛╨│╨╛ ╤А╤П╨┤╨░ тАФ ╨│╨░╨╖╤Л, ╨б5тАФ╨б16 тАФ ╨╢╨╕╨┤╨║╨╛╤Б╤В╨╕, ╨╜╨░╤З╨╕╨╜╨░╤П ╤Б ╨б17 ╨╕ ╨▓╤Л╤И╨╡ тАФ ╤В╨▓╨╡╤А╨┤╤Л╨╡ ╨▓╨╡╤Й╨╡╤Б╤В╨▓╨░. ╨в╨╡╨╝╨┐╨╡╤А╨░╤В╤Г╤А╤Л ╨║╨╕╨┐╨╡╨╜╨╕╤П ╨╕ ╨┐╨╗╨░╨▓╨╗╨╡╨╜╨╕╤П ╤Ж╨╕╨║╨╗╨╛╨░╨╗╨║╨░╨╜╨╛╨▓ ╨╜╨╡╤Б╨║╨╛╨╗╤М╨║╨╛ ╨▓╤Л╤И╨╡, ╤З╨╡╨╝ ╤Г ╨░╨╗╨║╨░╨╜╨╛╨▓ ╨┐╤А╨╕ ╨╛╨┤╨╕╨╜╨░╨║╨╛╨▓╨╛╨╝ ╤З╨╕╤Б╨╗╨╡ ╨░╤В╨╛╨╝╨╛╨▓ ╤Г╨│╨╗╨╡╤А╨╛╨┤╨░.
╨Я╨╛╨╗╤Г╤З╨╡╨╜╨╕╨╡. ╨Ю╨▒╤Й╨╕╨╝ ╤Б╨┐╨╛╤Б╨╛╨▒╨╛╨╝ ╨┐╨╛╨╗╤Г╤З╨╡╨╜╨╕╤П ╤Ж╨╕╨║╨╗╨╛╨░╨╗╨║╨░╨╜╨╛╨▓ ╤П╨▓╨╗╤П╨╡╤В╤Б╤П ╨┤╨╡╨╣╤Б╤В╨▓╨╕╨╡ ╨╝╨╡╤В╨░╨╗╨╗╨╛╨▓ ╨╜╨░ ╨┤╨╕╨│╨░╨╗╨╛╨│╨╡╨╜╨╛╨┐╤А╨╛-╨╕╨╖╨▓╨╛╨┤╨╜╤Л╨╡ ╨░╨╗╨║╨░╨╜╨╛╨▓:
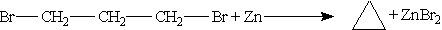
╨б╨╛╨╡╨┤╨╕╨╜╨╡╨╜╨╕╤П ╤А╤П╨┤╨░ ╤Ж╨╕╨║╨╗╨╛╨│╨╡╨║╤Б╨░╨╜╨░ ╨┐╨╛╨╗╤Г╤З╨░╤О╤В ╨│╨╕╨┤╤А╨╕╤А╨╛╨▓╨░╨╜╨╕╨╡╨╝ ╨░╤А╨╛╨╝╨░╤В╨╕╤З╨╡╤Б╨║╨╕╤Е ╤Г╨│╨╗╨╡╨▓╨╛╨┤╨╛╤А╨╛╨┤╨╛╨▓, ╨╜╨░╨┐╤А╨╕╨╝╨╡╤А:
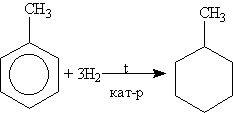
╨е╨╕╨╝╨╕╤З╨╡╤Б╨║╨╕╨╡ ╤Б╨▓╨╛╨╣╤Б╤В╨▓╨░. ╨Т ╤Б╤В╤А╨╛╨╡╨╜╨╕╨╕ ╤Ж╨╕╨║╨╗╨╛╨░╨╗╨║╨░╨╜╨╛╨▓ ╨╕╨╝╨╡╨╡╤В╤Б╤П ╤А╤П╨┤ ╨╛╤Б╨╛╨▒╨╡╨╜╨╜╨╛╤Б╤В╨╡╨╣, ╨╛╨┐╤А╨╡╨┤╨╡╨╗╤П╤О╤Й╨╕╤Е ╨╕╤Е ╤Е╨╕╨╝╨╕╤З╨╡╤Б╨║╨╕╨╡ ╤Б╨▓╨╛╨╣╤Б╤В╨▓╨░. ╨Ь╨░╨╗╤Л╨╡ ╤Ж╨╕╨║╨╗╤Л (╨╛╤Б╨╛╨▒╨╡╨╜╨╜╨╛ ╤Ж╨╕╨║╨╗╨╛╨┐╤А╨╛╨┐╨░╨╜) ╨╜╨╡╤Г╤Б╤В╨╛╨╣╤З╨╕╨▓╤Л ╨╕ ╤Б╨┐╨╛╤Б╨╛╨▒╨╜╤Л ╨║ ╤А╨░╨╖╤А╤Л╨▓╤Г, ╨┐╨╛╤Н╤В╨╛╨╝╤Г ╨╛╨╜╨╕ ╤Б╨║╨╗╨╛╨╜╨╜╤Л ╨║ ╤А╨╡╨░╨║╤Ж╨╕╤П╨╝ ╨┐╤А╨╕╤Б╨╛╨╡╨┤╨╕╨╜╨╡╨╜╨╕╤П, ╨╜╨░╨┐╨╛╨╝╨╕╨╜╨░╤П ╨╜╨╡╨╜╨░╤Б╤Л╤Й╨╡╨╜╨╜╤Л╨╡ ╤Б╨╛╨╡╨┤╨╕╨╜╨╡╨╜╨╕╤П. ╨в╨░╨║, ╤Ж╨╕╨║╨╗╨╛╨┐╤А╨╛╨┐╨░╨╜ ╨┐╤А╨╕╤Б╨╛╨╡╨┤╨╕╨╜╤П╨╡╤В ╨▒╤А╨╛╨╝ ╤Б ╤А╨░╨╖╤А╤Л╨▓╨╛╨╝ ╤Ж╨╕╨║╨╗╨░, ╨╛╨▒╤А╨░╨╖╤Г╤П 1,3-╨┤╨╕╨▒╤А╨╛╨╝╨┐╤А╨╛╨┐╨░╨╜ (╤А╨╡╨░╨║╤Ж╨╕╤П ╨╕╨┤╨╡╤В ╤В╤А╤Г╨┤╨╜╨╡╨╡, ╤З╨╡╨╝ ╤Б ╨┐╤А╨╛╨┐╨╡╨╜╨╛╨╝):
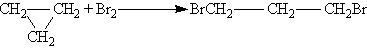
╨Ю╨▒╤Л╤З╨╜╤Л╨╡ ╤Ж╨╕╨║╨╗╤Л ╨╛╤З╨╡╨╜╤М ╤Г╤Б╤В╨╛╨╣╤З╨╕╨▓╤Л ╨╕ ╨▓╤Б╤В╤Г╨┐╨░╤О╤В ╤В╨╛╨╗╤М╨║╨╛ ╨▓ ╤А╨╡╨░╨║╤Ж╨╕╨╕ ╨╖╨░╨╝╨╡╤Й╨╡╨╜╨╕╤П, ╨┐╨╛╨┤╨╛╨▒╨╜╨╛ ╨░╨╗╨║╨░╨╜╨░╨╝:
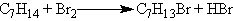
|



